ProtheraCytes®
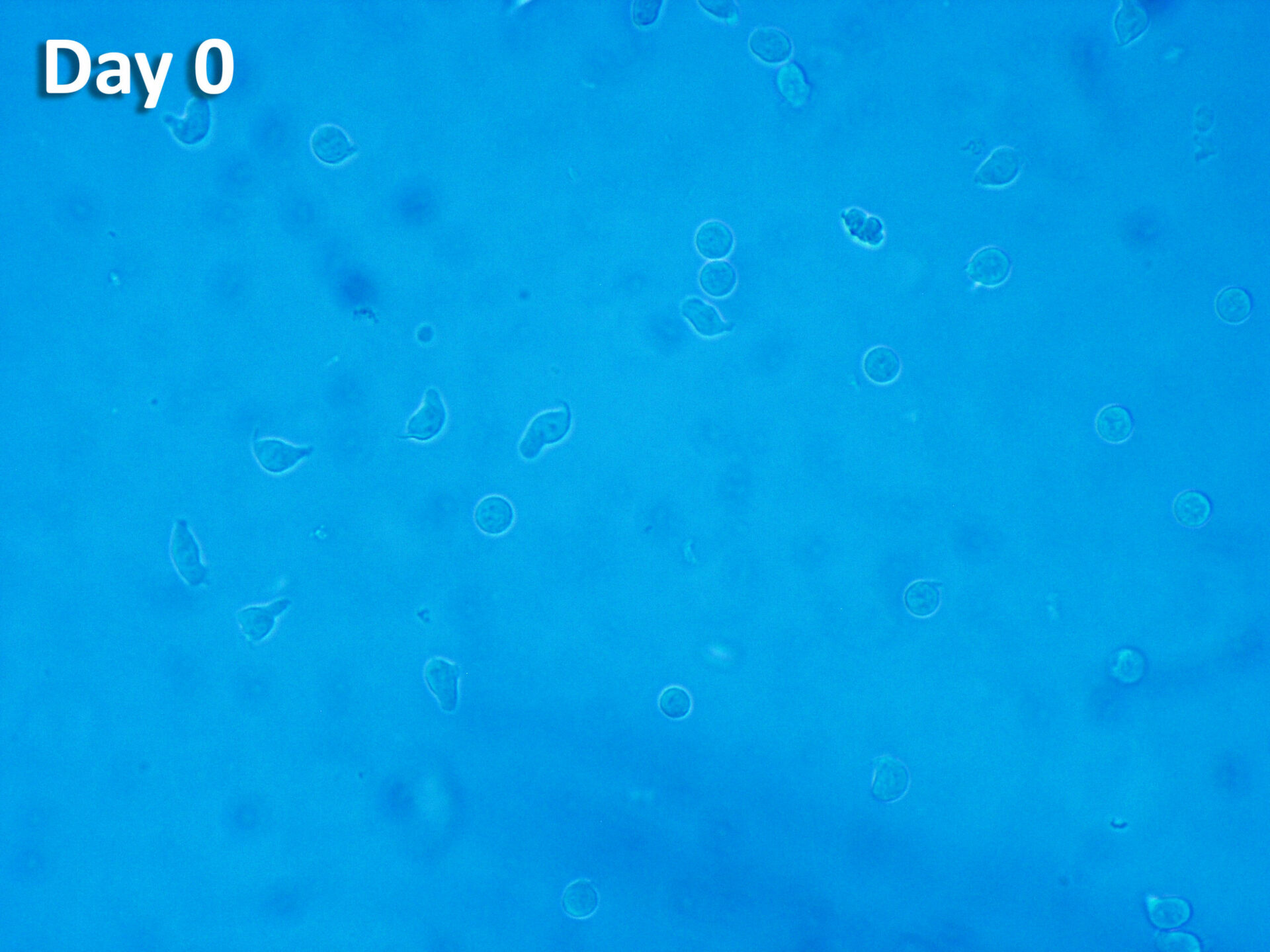
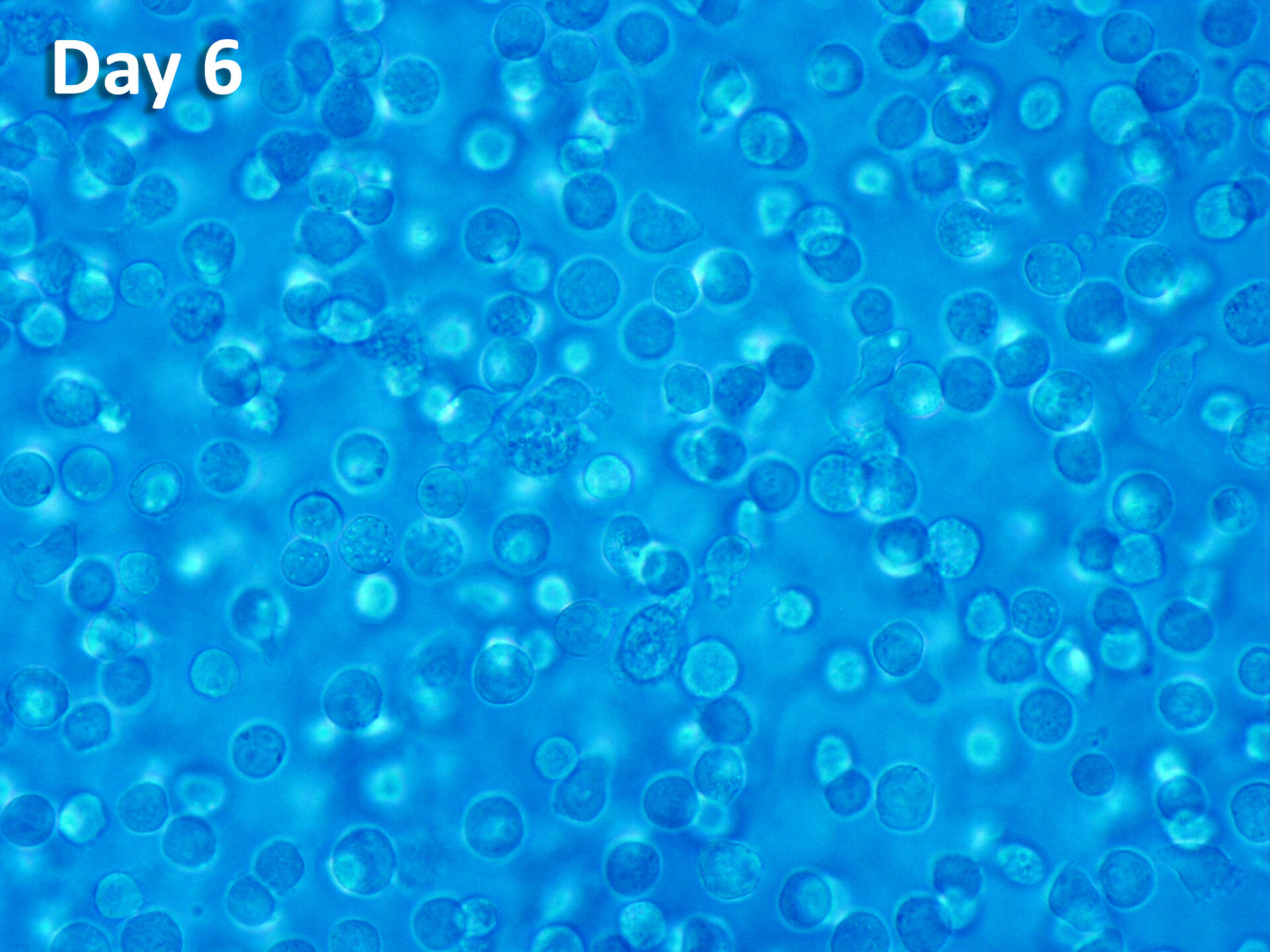
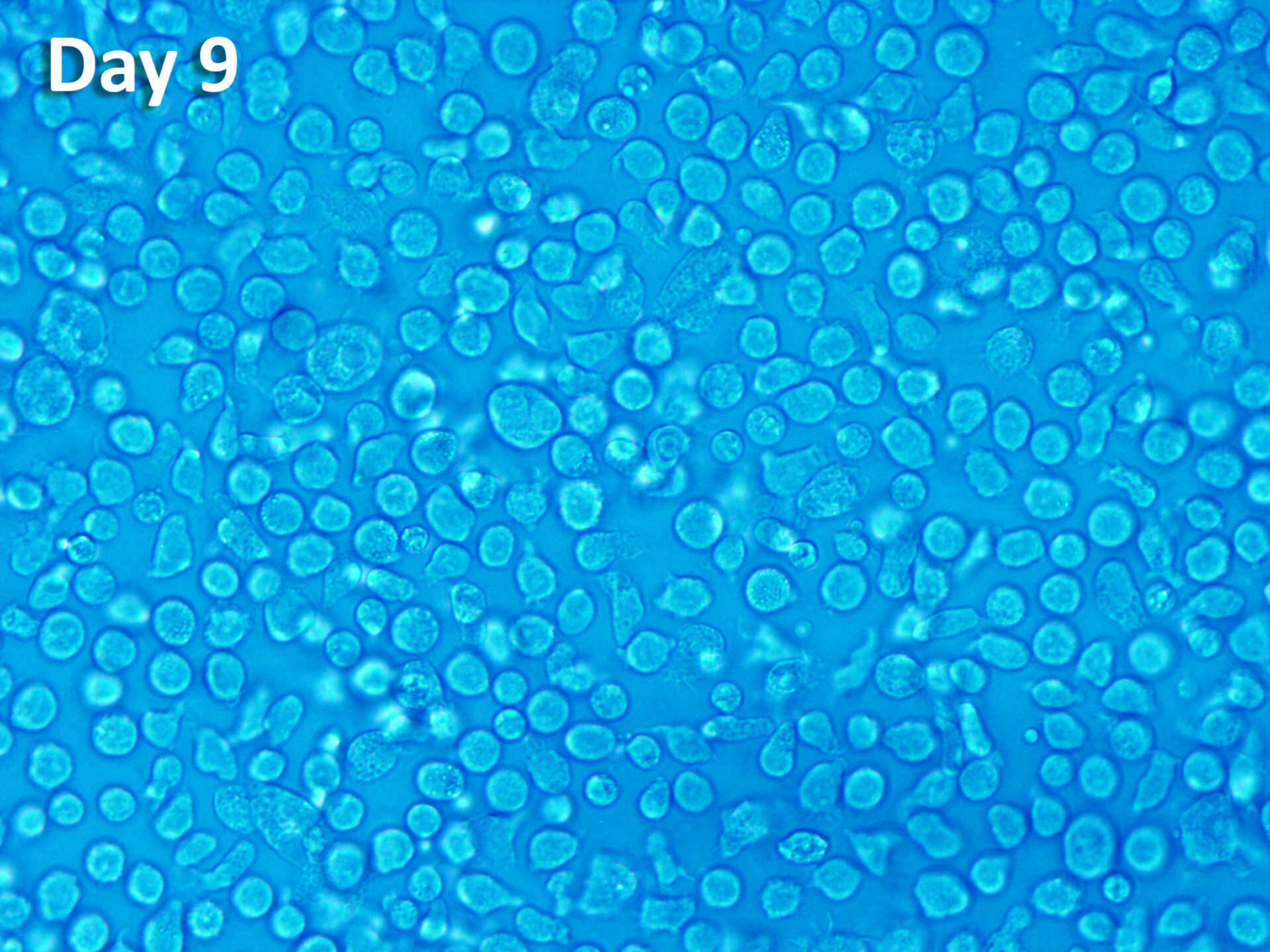
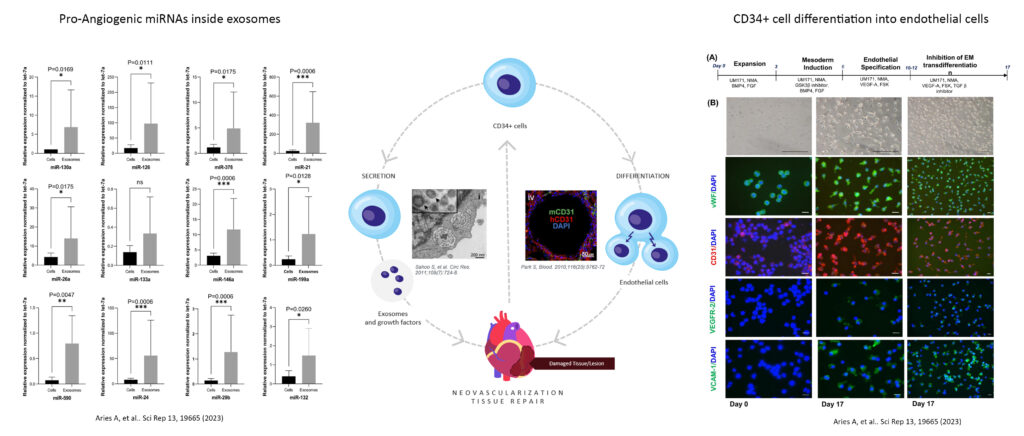
ProtheraCytes® est un bio-médicament dérivé de cellules souches CD34+ prélevées dans le sang périphérique du patient après leur mobilisation à partir de la moelle osseuse, et obtenu par une technologie de multiplication, de purification et de formulation cellulaires propriétaires. Ce bio-médicament se présente sous forme d'une suspension cellulaire prête à injecter. Il a le potentiel de régénérer divers tissus endommagés, y compris le tissu cardiaque.